Сайт-селективный мониторинг синтеза белка Labeling of Nascent Proteins - Puromycin-based Fluorescent & Biotin Labeling
|
 |
O-Пропаргил пуромицин: нерадиоактивный мониторинг начинающегося синтеза белка.
Динамика общего белкового синтеза (как пространственная, так и временная) - существенный параметр для характеристики клеточного ответа на разнообразные физиологические и патологические условия. Современные исследования клеточного белкового синтеза полагаются на косвенные методы такие, как ДНК- и мРНК микрочипы или классическое радиоактивное мечение метаболитов 35S-метионином.
Лю с соавторами описывает нерадиоактивную альтернативу анализа вновь синтезируемых белков в клеточных культурах и организмах, базирующегося на алкин-аналоге пуромицина (Рис. 1). Клеточно-проницаемый O-Пропаргил пуромицин (Рис. 1A) встраивается в C-конец транслируемой полипептидной цепи, таким образом останавливая трансляцию.
Возникающий С-концевой алкин-меченый белок может детектироваться при помощи Cu(I)-катализируемой клик-реакции, которая предлагает на выбор внедрение биотиновой группы (Азиды Биотина) для последующей очистки или флюоресцентной группы (Азиды флюоресцентных красителей) для последующей визуализации под микроскопом [1,2,3].
В отличие от упомянутого ранее аналогичного подхода на основе нерадиоактивного метионина [4,5], для основанного на О-Пропаргил пуромицине мониторинга синтеза белка не требуется чистая от метионина среда.
Лю с соавторами описывает нерадиоактивную альтернативу анализа вновь синтезируемых белков в клеточных культурах и организмах, базирующегося на алкин-аналоге пуромицина (Рис. 1). Клеточно-проницаемый O-Пропаргил пуромицин (Рис. 1A) встраивается в C-конец транслируемой полипептидной цепи, таким образом останавливая трансляцию.
Возникающий С-концевой алкин-меченый белок может детектироваться при помощи Cu(I)-катализируемой клик-реакции, которая предлагает на выбор внедрение биотиновой группы (Азиды Биотина) для последующей очистки или флюоресцентной группы (Азиды флюоресцентных красителей) для последующей визуализации под микроскопом [1,2,3].
В отличие от упомянутого ранее аналогичного подхода на основе нерадиоактивного метионина [4,5], для основанного на О-Пропаргил пуромицине мониторинга синтеза белка не требуется чистая от метионина среда.
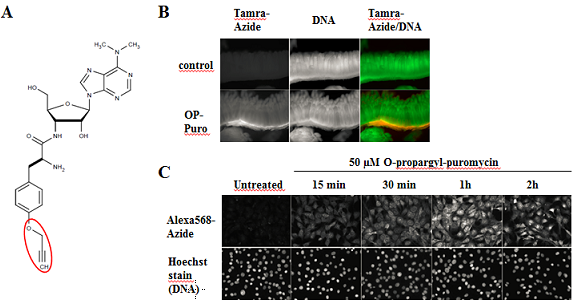 |
B) Экспрессия образующихся белков в углублениях тонкой кишки мыши визуализированы тотальным окрашиванием препарата. Белки, меченые О-Пропаргил пуромицином детектируются Тетраметилродамин-азидом (Tamra-азид) (красный) и ядерная ДНК окрашена OliGreen (зеленый) (изменено в соответствии с [1])
C) Вновь синтезированные белки в клетках NIH3T3 напрямую определяются инкубацией с 50 μM OP-puro. Белки, меченые OP-puro визуализированы Alexa568-азидом, ядерная ДНК окрашена красителем Hoechst (изменено в соответствии с [1]).
Литература:
[1] Liu et al. (2012) Imaging protein synthesis in cells and tissues with an alkyne analog of puromycin. Proc. Natl. Acad. Sci. USA 109(2):413.
[2] Goodman et al. (2012) Imaging of protein synthesis with puromycin. Proc Natl Acad Sci USA 109(17):E989.
[3] Salic et al. (2012) Reply to Goodman et al.: Imaging protein synthesis with puromycin and the subcellular localization of puromycin-polypeptide conjugates. Proc. Natl. Acad. Sci. USA 109(17):E990.
[4] Dieterich et al. (2010) In situ visualization and dynamics of newly synthesized proteins in rat hippocampal neurons. Nature Neuroscience 13(7): 897.
[5] Dieck et al. (2012) Metabolic Labeling with Noncanonical Amino Acids and Visualisation by Chemoselective Fluorescent Tagging. Current Protocols in Cell Biology 7:7.11.1.
[2] Goodman et al. (2012) Imaging of protein synthesis with puromycin. Proc Natl Acad Sci USA 109(17):E989.
[3] Salic et al. (2012) Reply to Goodman et al.: Imaging protein synthesis with puromycin and the subcellular localization of puromycin-polypeptide conjugates. Proc. Natl. Acad. Sci. USA 109(17):E990.
[4] Dieterich et al. (2010) In situ visualization and dynamics of newly synthesized proteins in rat hippocampal neurons. Nature Neuroscience 13(7): 897.
[5] Dieck et al. (2012) Metabolic Labeling with Noncanonical Amino Acids and Visualisation by Chemoselective Fluorescent Tagging. Current Protocols in Cell Biology 7:7.11.1.
| |||||||||||||||||||
| |||||||||||||||||||
Информация представлена исключительно в ознакомительных целях и ни при каких условиях не является публичной офертой



 Datasheet
Datasheet




